Wegweiser Regulatorik Gesundheitswirtschaft BW
| Die Anlaufstelle Regulatorik Gesundheitswirtschaft BW ist Ihr Lotse für einen sicheren Weg durch das Labyrinth der Regularien. Das bieten wir Informationen von "A" wie Arzneimittel-Lieferengpässe über "P" wie PFAS bis "Z" wie Zulassung für Arzneimittel und Medizinprodukte: Steckbriefe Fachartikel und Podcast Orientierungshilfen und Leitfäden Informationsveranstaltungen Kontakt zu Behörden, Benannten Stellen, Regierungspräsidien, Clustern und Netzwerken
So erreichen Sie uns Sie erreichen uns per E-Mail unter regulatorik-gesundheitswirtschaft(at)bio-pro.de. |
Innovation trifft Regulatorik – wir hören zu!
Regulatorik soll Innovationen nicht bremsen, sondern begleiten – und dafür möchten wir wissen, wo Sie aktuell stehen.
Welche Themen beschäftigen Sie zurzeit? Und wo wünschen Sie sich mehr Orientierung oder Austausch?
Ihr Rückmeldungen zeigen uns, wo Handlungsbedarf besteht – und helfen uns, praxisnahe Angebote gezielt weiterzuentwickeln.
Schreiben Sie uns an regulatorik-gesundheitswirtschaft@bio-pro.de.
Aktuelles auf einen Blick
Veranstaltungen
Die Veranstaltungsreihe "Regulatorik Nachgefragt" beleuchtet aktuelle und zukünftige Regularien mit Relevanz für die Gesundheitsindustrie und wird in regelmäßigen Abständen als Online-Veranstaltung angeboten.
Umfragen
Ihre Einschätzung ist uns wichtig!
Als Landesagentur und zentrale Ansprechpartnerin für die Gesundheitswirtschaft im Land ist es uns ein wichtiges Anliegen, aktuelle Entwicklungen und Herausforderungen zu verstehen und gemeinsam mit den Akteurinnen und Akteuren der Branche weiterzuentwickeln.
Regulatorische Fragestellungen rund um nachhaltige Ansätze in der Gesundheitswirtschaft und zirkuläres Wirtschaften gewinnen an Bedeutung und haben in vielen Unternehmen operative wie strategische Auswirkungen.
Ihre Rückmeldung hilft uns, Themen zu priorisieren und passende Informations- und Austauschformate zu entwickeln.
Datenbanken

Sie benötigen Informationen zu Regularien, die Ihr Unternehmen im Bereich der Gesundheitswirtschaft betreffen? Der Regulatorik-Lotse der BIOPRO Baden-Württemberg GmbH stellt hier eine Auswahl an aktuellen und zukünftig relevanten Regularien in Form von Steckbriefen zur Verfügung. Diese sollen Ihnen dabei helfen, sich einen schnellen Überblick zu den regulatorischen Anforderungen zu verschaffen.

Sie suchen nach einem passenden Studienzentrum für Ihre Klinische Prüfung? Dann ist der KlinischeStudien (KS)-Lotse BW genau das richtige für Sie!
Der KS-Lotse stellt baden-württembergische Studienzentren für Klinische Studien mit Medizinprodukten und/oder In-vitro-Diagnostika vor.
Fachartikel
-
Zusätzliche Reinigungsstufe in Kläranlagen - 03.07.2025
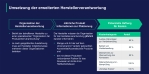
Die Neuauflage der EU-Kommunalabwasserrichtlinie KARL führt eine vierte Reinigungsstufe für Kläranlagen ein und bittet Hersteller von Arzneimitteln und Kosmetika zur Kasse. Sie tragen mindestens 80 Prozent der Kosten für den Ausbau der Abwasseranlagen.
-
Preisbildungsprozess bei neuen Arzneimitteln - 03.06.2025
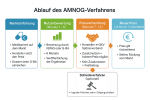
Das Arzneimittelmarktneuordnungsgesetz (AMNOG) ist maßgeblich für den Preis, zu dem neue Medikamente auf den deutschen Markt kommen. Das Verfahren soll vor allem dafür sorgen, dass der Zusatznutzen neuer Wirkstoffe für die Patientinnen und Patienten im Fokus steht. Ein System mit Vor- und Nachteilen.
News
Bekanntmachung des Bundesministeriums für Bildung und Forschung
Mit dieser Förderrichtlinie beabsichtigt das BMBF, die Validierung neuer Methoden im regulatorischen Kontext zu fördern mit dem Ziel, neue tierversuchfreie, für den Menschen relevante Methoden als OECD-Prüfrichtlinien einzuführen oder qualifizierte Modelle für die Wirksamkeitsprüfung neuer Arzneimittel zu etablieren.
-
Diskussionspapiere und Gutachten als praxisnahe Hilfestellungen - 26.01.2026

Die Landesagentur BIOPRO Baden-Württemberg stellt Unternehmen sowie Akteurinnen und Akteuren der Gesundheitswirtschaft ab sofort praxisnahe Diskussionspapiere und Gutachten zu aktuellen regulatorischen Fragestellungen bereit. Die Veröffentlichungen sind Teil des Projekts Anlaufstelle Regulatorik Gesundheitswirtschaft BW, das vom Ministerium für Wirtschaft, Arbeit und Tourismus Baden-Württemberg gefördert wird.
-
Pressemitteilung - 22.01.2026
Weil die europäische Kommunalabwasserrichtlinie (KARL) in ihrer jetzigen Form weiterhin eine Bedrohung des Pharmastandortes Europa darstellt und auch bei der Arzneimittelversorgung in Deutschland für Einschränkungen sorgen könnte, bleibt sie eines der wichtigsten europapolitischen Themen von Pharma Deutschland.
-
Pressemitteilung - 20.01.2026
Gesundheitsminister Manne Lucha begrüßt den Start der Verhandlungen zum EU-Gesetz über kritische Arzneimittel. Der Critical Medicines Act bietet wichtige Ansatzpunkte, um die Versorgungssicherheit zu stärken und Europa krisenfester zu machen.